
Těhotenství je spojeno se změnami téměř všech orgánových systémů. Fyziologické, biochemické a anatomické změny odrážejí jak adaptaci organismu ženy na nároky vyvíjejícího se plodu, tak adaptační změny zabraňující poškození mateřského organismu v průběhu těhotenství, porodu nebo šestinedělí. Adaptační změny organismu indukované těhotenstvím jsou obvykle reverzibilní a vracejí se opět na původní úroveň před těhotenstvím za několik měsíců po porodu nebo ukončení laktace. Porozumění fyziologii organismu během těhotenství je nezbytné pro odpovídající lékařskou péči o těhotné ženy ve zdraví i nemoci.
1. Kardiovaskulární systém
Postavení a velikost srdce
Při zvětšování dělohy v průběhu těhotenství je elevována bránice a srdce je vytlačováno kraniálně a doleva s posunem podélné osy srdeční horizontálně, tzn. že úder hrotu srdečního je pozorován více laterálně. Objem srdeční se zvětšuje asi o 12 % s největším objemem ve III. trimestru a srdeční sval hypertrofuje. Následkem změn polohy srdce nastávají i změny na EKG. Elektrická osa srdeční se sklání o 15–20 stupňů doleva, nastávají reverzibilní změny úseku ST a vlny T a Q. Vlna T je ve III. svodu plochá nebo negativní a v končetinových a hrudních svodech pozorujeme depresi úseku ST. Někdy zjišťujeme nízkou voltáž komplexu QRS a hluboké Q ve III. svodu. V těhotenství jsou častěji pozorovány extrasystoly a záchvaty supraventrikulární paroxyzmální tachykardie.
Srdeční výdej
Srdeční výdej je dán součinem tepového objemu a tepové frekvence a zvyšuje se v průběhu těhotenství asi o 40 % (tab. 1). Tento stav se významně nemění až do třetího poporodního dne. Srdeční výdej se zvyšuje od 8. týdne těhotenství, ve 30.–34. týdnu těhotenství dosahuje maxima (9 l/min) a nemění se až do porodu. Srdeční výdej se mění v závislosti na poloze těhotné ženy. Těhotná děloha stlačuje dolní dutou žílu, tím se snižuje žilní návrat a v důsledku toho i srdeční výdej (zejména v poloze na zádech). Za porodu se srdeční výdej zvyšuje o 40 % v porovnání se stavem na konci těhotenství. Na začátku těhotenství se srdeční výdej zvyšuje pouze zvýšením tepového objemu s maximem zvýšení o 25–30 % ve 12.–24. týdnu. V poloze na zádech po 20. týdnu těhotenství se tepový objem snižuje a blíží se k hodnotám u netěhotných. V poloze na boku se tepový objem nemění. Tepová frekvence se zvyšuje až v průběhu těhotenství a na jeho konci je až o 15 úderů/min vyšší než u netěhotné ženy. První ozva může být rozštěpena a obě části hlasitější. Až 90 % těhotných žen má systolický šelest v důsledku zvýšeného tepového objemu.
| Parametr | Změna (%) |
| Celkový objem krve | +40 |
| Plazmatický objem | +45 |
| Počet erytrocytů | +20-40 |
| Srdeční výdej | +40 |
| Tepový objem | +30 |
| Srdeční frekvence | +15-20 |
Krevní tlak
Krevní tlak je v průběhu těhotenství o něco nižší než u netěhotných. Systolický tlak se snižuje jen nepatrně, diastolický o 5–10 mmHg (0,7–1,3 kPa) od 12. do 26. týdne. Po 36. týdnu se diastolický tlak vrací k hodnotám před těhotenstvím. Krevní tlak měřený manometrem s manžetou, která obepíná a. brachialis, se mění hlavně ve druhé polovině těhotenství, v závislosti na poloze ženy. Nejvyšší tlak je v poloze vsedě, nižší je vleže na zádech a ještě o něco nižší je v poloze vleže na boku. V průběhu těhotenství se významně zvyšuje tlak ve vénách dolních končetin, vulvy a rekta v poloze vestoje, vleže na zádech a vsedě. Venózní tlak je vyšší ve femorální véně, na jejíž straně je uložena placenta. Průměrný rozdíl je asi 27 mmH2O (0,3 kPa). Zvýšený venózní tlak často způsobuje i vznik hemoroidů a je jednou z hlavních příčin vzniku edémů dolních končetin. Zvýšený venózní tlak je způsoben tlakem těhotné dělohy na v. cava inferior a vv. iliacae. Komprese těchto vén způsobuje i oblenění průtoku krve kaudálně od místa komprese, a to je jeden z rizikových faktorů pro vznik trombózy v těhotenství. Výsledný účinek komprese v. cava inferior je poněkud zmírněn vznikem paravertebrálního kolaterálního oběhu. V horní polovině těla se v těhotenství venózní tlak nemění. Ve III. trimestru může zvětšená děloha částečně komprimovat aortu a její větve. Následkem této komprese je krevní tlak v a. femoralis nižší než v a. brachialis. Stlačení aorty se zvyšuje při kontrakci a při poloze ženy vleže na zádech, průtok krve dělohou se tak snižuje a rozvíjí se distres plodu. Tento jev se někdy nazývá Poseirův efekt. V období termínu porodu v poloze vleže na zádech nastává u 10 % žen velmi významný pokles krevního tlaku spojený s nauzeou, závratí a někdy dokonce i srdeční synkopou. Příčina je v téměř kompletním uzávěru dolní duté žíly komprimované těhotnou dělohou u žen s vrozeně nedostatečnou kolaterální cirkulací. Tento stav je doprovázen tachykardií matky a snížením srdečního výdeje a označuje se jako syndrom venae cavae inferior. Při děložní kontrakci se za porodu zvyšuje střední arteriální krevní tlak v průměru o 10 mmHg (1,3 kPa).
Průtok krve v jednotlivých systémech
V těhotenství se průtok krve zvyšuje zejména v děloze (viz odst. 6 ), v ledvinách, v prsech a kůži. Zvýšení průtoku záleží na délce těhotenství. V ledvinách se zvyšuje průtok krve v průměru o 400 ml/min ve srovnání s průtokem před těhotenstvím a v prsech o 200 ml/min. Velké zvýšení průtoku krve zjišťujeme také v kůži rukou a nohou. Kůže bývá v těchto místech obvykle teplejší, někdy je studeně vlhká. Prostřednictvím zvýšeného průtoku krve kůží se uvolňuje teplo produkované plodem a zvýšeným metabolismem matky v těhotenství. Zvyšuje se i prokrvení sliznic, což vede k jejich edematóznímu prosáknutí (dýchací cesty). Při fyzické námaze se následkem redistribuce krve do svalů snižuje průtok krve fetoplacentární jednotkou. U zdravé matky a plodu neovlivňuje mírná až středně těžká fyzická práce vývoj plodu.
2. Objemy tělesných tekutin a hematologický systém
U těhotné ženy se zvětšuje objem extracelulární tekutiny (intravaskulární a intersticiální kompartment) a vzniká fyziologická extracelulární hypervolémie. Objem intersticiálního kompartmentu se v těhotenství postupně zvětšuje a dosahuje maxima ve III. trimestru.
Objem plazmy
Objem plazmy se zvětšuje s velikostí plodu – čím větší plod, tím větší plazmatický objem. Její objem se rovněž zvětšuje v závislosti na výšce ženy, počtu a četnosti těhotenství. U malých žen se objem plazmy zvětšuje asi o 20 %, u vysokých žen až o 100 %, průměrné zvětšení objemu je asi 50 %, tj. 1250–1400 ml. Hypervolémie začíná již v 6. týdnu, nejrychlejší nárůst je ve II. trimestru a od 30. týdne je vzestup jen nepatrný. Některé studie dokonce prokázaly nepatrné zmenšování objemu plazmy v posledních 10 týdnech těhotenství. U žen s opakovanými potraty, předčasnými porody a s preeklampsií se zvětšuje objem plazmy jen nepatrně nebo vůbec ne. Protože se objem plazmy zvětšuje dvakrát více než objem erytrocytární masy, snižuje se koncentrace hemoglobinu a hematokrit – vzniká tzv. diluční anémie (nutno odlišit od skutečné anémie v těhotenství, která je nejčastěji sideropenická, méně často megaloblastická). Mechanismus těchto změn není zcela jasný, ale uplatňuje se zde zvýšená produkce aldosteronu, estrogenů, progesteronu a atriálního natriuretického peptidu. Zvýšený objem plazmy (a tím i krve) v těhotenství je nutný při zvýšeném průtoku krve některými orgány (děloha, ledviny, kůže, prsy) a pro kompenzaci ztrát krve při porodu. Ztráta krve při spontánním porodu se odhaduje na 400–600 ml a při císařském řezu okolo 1000 ml.
Erytrocyty
Objem erytrocytární masy se zvýší u těhotné ženy s jedním plodem ze 1400 ml na 1650 ml, tj. o 250 ml neboli o 18 %. Při podávání preparátů železa se objem erytrocytární masy zvyšuje o dalších 150–200 ml, tj. celkem o 400–450 ml (30 %). Toto množství erytrocytů obsahuje 475 mg Fe. U vícečetných těhotenství je objem erytrocytární masy větší než u jednočetných. Počet erytrocytů klesá ze 4,5 × 1012/l před těhotenstvím na hodnoty 3,7 × 1012/l ve 30. týdnu, kdy je jejich počet nejnižší. Později se již počet erytrocytů nemění nebo nepatrně stoupá. Koncentrace hemoglobinu klesá ze 137–140 g/l před těhotenstvím na 110–120 g/l na konci těhotenství. Podobné snížení nastává u hematokritu, který klesá z hodnot okolo 0,40 na 0,33–0,35. Pro ženy bílé rasy je v těhotenství z hlediska hemodynamického (viskozita krve) a z hlediska přenosové kapacity krve pro kyslík nejvhodnější hematokrit 0,35, arterio-venózní diference je v těhotenství menší než před těhotenstvím. Těhotenství je v dospělosti jediný fyziologický stav, ve kterém je v organismu přítomen fetální hemoglobin (HbF) a zmnožené F-buňky (erytrocyty obsahující HbF). Nejvyšších hodnot dosahují mezi 10.–12. a 18.–22. týdnem těhotenství a normalizují se do 8. postpartálního týdne. Tento HbF pochází od matky, nikoli od fétu. Zmnožení F-buněk koreluje s hladinami HCG a je indukovatelné erytropoetinem.
Železo
Zdravá žena přijímá denně potravou 12–18 mg železa (Fe) a z toho se vstřebává přibližně 5–10 %. Absorpce Fe se zvyšuje při jeho deficitu, a to na 20–50 %. Absorpce Fe se zvyšuje také v těhotenství, ve II. trimestru na 30 %, ve III. až na 40 %. Průměrná denní ztráta Fe u netěhotné ženy je 1–2 mg, u těhotné 0,75 mg, tj. za těhotenství celkem 200 mg. V těhotenství je část Fe matky transportováno do placenty a plodu. Nastává snížení zásob Fe u matky a tento stav může vyústit v deficit Fe, event. až v anémii z nedostatku Fe (sideropenická anémie). Fe se dostává k plodu aktivním transportem přes placentu. Fe je transportováno pouze jedním směrem – od matky k plodu, a to i od matek s deficitem Fe a sideropenickou anémií. Přesný mechanismus transportu Fe přes placentu neznáme. Přísun Fe do placenty a plodu není v průběhu těhotenství rovnoměrný, od 4. měsíce do porodu kolísá v rozmezí 0,5–5,0 mg/24 h. V těhotenství se spotřebuje asi 500 mg Fe na zvětšení celkového objemu erytrocytární masy u matky. V období porodu obsahuje plod okolo 300 mg Fe ve formě hemoglobinu a zásobního Fe uloženého v játrech. V placentě je uloženo dalších 30–100 mg Fe. Na druhé straně v důsledku amenorey v těhotenství a laktaci „ušetří“ žena 250–300 mg Fe. Ztráty Fe v mléce nejsou významné. Při spontánním porodu se ztrácí cca 600 ml krve, a to při hematokritu 0,37 představuje přibližně ztrátu 250 mg Fe. Při malé ztrátě krve při porodu se v šestinedělí snižuje objem erytrocytární masy, tím se redukuje množství celkového hemoglobinu a část Fe z tohoto hemoglobinu se ukládá jako zásobní ve formě feritinu (mobilizovatelné – lze jej využít pro potřeby organismu ) a hemosiderinu (nemobilizovatelné). Z toho, co bylo uvedeno výše, je zřejmé, že v těhotenství se spotřeba Fe zvyšuje a že v těhotenství a po porodu vzniká často v důsledku zvýšené spotřeby Fe a krevní ztráty sideropenie, event. sideropenická anémie.
Leukocyty
Celkový počet bílých krvinek se v těhotenství zvyšuje až na 12,0 × 109/l, ve III. trimestru byly zjištěny i hodnoty 16,0 × 109/l. Za porodu dosahuje počet leukocytů i 25–30 × 109/l. Počet lymfocytů a monocytů je relativně stabilní, zvyšuje se počet polymorfonukleárů. Počet bazofilů nepatrně klesá. Eozinofily se u některých těhotných zvyšují, u jiných snižují nebo se jejich počet nemění; příčina není známá.
Trombocyty
Počet trombocytů se v těhotenství významně nemění, event. může nepatrně klesat a pohybuje se v rozmezí normálních hodnot u netěhotných žen, tj. 140–400 × 109/l. V těhotenství se zvyšuje trombocytopoéza, ale i konzumpce destiček. Rovněž se zvyšuje koncentrace prostacyklinu (inhibitor agregace destiček) a tromboxanu A2 (vyvolává vazokonstrikci a agregaci destiček). Během těhotenství se dvakrát zvyšuje riziko venózní trombembolie.
Sedimentace erytrocytů
V těhotenství se sedimentace (FW) zvyšuje na 44 až 114 mm/h s průměrem 78 mm. Příčinou vysoké sedimentace je zvýšená hladina plazmatických globulinů a fibrinogenu. Sedimentace nemá v těhotenství diagnostickou hodnotu.
Viskozita krve
Změny v počtu erytrocytů ovlivňují viskozitu krve. Při srovnání s destilovanou vodou je viskozita krve před těhotenstvím 4,6, na začátku těhotenství pak činí 4,2 a v době nejnižšího počtu červených krvinek, tj. ve 30. týdnu, je viskozita 3,8. Snížení viskozity krve má za následek snížení srdeční práce a je jedním z faktorů, který způsobuje snížení krevního tlaku při zvýšeném srdečním výdeji.
Elekrolyty v séru
Na+ – koncentrace klesá o 2–3 mmol/l (130–148 mmol/l) K+ – koncentrace klesá o 0,2–0,3 mmol/l (3,8–5,1 mmol/l) Ca2+ – koncentrace klesá o 10 % (2,25–2,75 mmol/l) Mg2+ – koncentrace klesá o 10–20 % (0,75–1,25 mmol/l) Koncentrace Cl- a fosforu se výrazně nemění (98–106 a 0,65–1,62 mmol/l). V závorce jsou uvedena rozpětí normálních hodnot u netěhotných žen.
Srážení krve
V průběhu těhotenství jsou změněny hladiny nebo aktivita jak faktorů plazmatického koagulačního systému, tak faktorů fibrinolytického systému. Znalost mechanismů krevního srážení a fibrinolýzy je nesmírně důležitá, neboť umožňuje úspěšně léčit nejzávažnější porodnické komplikace – krvácení s event. následnou diseminovanou intravaskulární koagulopatií (DIC) a trombembolickou nemocí.
Plazmatický koagulační systém
Výsledkem aktivace kaskády plazmatického koagulačního systému (PKS) je konverze rozpustného fibrinogenu v pevný fibrin. Tato konverze se uskutečňuje prostřednictvím řady enzymových pochodů. Koncentrace fibrinogenu se zvyšuje v těhotenství o 1–2 g/l, tj. z 2–4,5 g/l na 4–6,5 g/l. Celkové množství fibrinogenu se zvyšuje z 10 g před těhotenstvím na 20 g na konci těhotenství. V průběhu normálního těhotenství se také signifikantně zvyšuje koncentrace faktorů VII (prokonvertin), VIII (antihemofilický faktor), IX (Christmas faktor) a X (Stuart-Prowerův faktor). Naopak hladiny faktorů II (protrombin), V (proakcelerin), XI (plasma tromboplastin antecedent) a XII (Hagemanův faktor) se téměř vůbec nemění. Přestože je těhotenství označováno za hyperkoagulační stav, ke spontánní intravaskulární koagulaci nedochází.
Fibrinolytický systém
Hladina plazminogenu se v plazmě během normálního těhotenství zvyšuje současně s koncentrací fibrinogenu, ale v důsledku snížené koncentrace aktivátoru plazminogenu se fibrinolytická aktivita snižuje. Na konci těhotenství se zvyšuje hladina fibrin-degradačních produktů (FDP). Hladina těchto látek se značně zvyšuje při abrupci placenty, při preeklampsii a eklampsii a mohou negativně ovlivnit aktivitu PKS.
3. Respirační systém
V těhotenství nastávají v respiračním systému anatomické změny, které částečně podmiňují změny funkční. Subkostální úhel je v časném těhotenství 68° a v době termínu porodu je zvětšen na 103°. Bránice se v těhotenství zvyšuje o 4 cm a příčný průměr hrudníku se rozšiřuje o 2 cm. Exkurze bránice se při dýchání zvyšuje o 1–1,5 cm. Dýchání je v graviditě spíše abdominální než kostální. V tab. 2 jsou uvedeny procentuální změny plicních objemů a plicních kapacit na konci těhotenství. Minutová ventilace plic stoupá od 10.–12. týdne těhotenství, ale zvětšuje se pouze dechový objem, zatímco dechová frekvence se nemění. Progesteron indukuje zvýšenou citlivost dechového centra na CO2 a to vede ke zvýšení dechového objemu. Změnou polohy bránice směrem nahoru se snižuje negativní intrapleurální tlak a nastává snížení funkční reziduální kapacity o 18 % (FRC je součet ERV a RV). Toto snížení se týká reziduálního objemu (RV) i exspiračního rezervního objemu (ERV). Přesto celková kapacita plic, vitální kapacita a inspirační kapacita zůstávají nezměněny, protože nastává kompenzatorní rozšíření příčného a předozadního průměru hrudníku. Po hlubokém výdechu se maximálně vydechnutý objem vzduchu (FEV) a maximální proudění vydechovaného vzduchu (PEF) nemění. To je způsobeno bronchodilatačním účinkem progesteronu, který vede ke snížení rezistence dýchacích cest. Plicní difúze (tj. výměna dýchacích plynů mezi alveolárním vzduchem a krví) je snížena o 15 %, pravděpodobně vlivem snížené koncentrace hemoglobinu matky a změnou kvality mukopolysacharidů v plicních kapilárách těhotné. Zvýšená spotřeba O2 je kompenzována proporčním zvýšením dynamických ventilačních parametrů.
| Parametr | Změna |
|
Mechanické parametry exkurze bránice exkurze hrudní stěny celková plicní rezistence plicní compliance FEV1 FEV1/FVC křivka průtok - objem |
zvýšena snížena -50% beze změn beze změn (obstrukce dýchacích cest) beze změn beze změn |
|
Plicní objemy IRV dechový objem ERV RV |
+ 5% + 45% - 25% - 15% |
|
Plicní kapacita inspirační kapacita FRC vitální kapacita celková plicní kapacita mrtvý prostor |
+ 15% - 20% beze změn - 5% + 45% |
|
Ventilační parametry dechová frekvence minutová ventilace alveolární ventilace uzavírací objem difúzní kapacita |
beze změn + 45% + 45% beze změn (kritérium obstrukčních změn) snížena kvalita alveolo-kapilární membrány |
4. Vylučovací systém
Pro těhotenství je charakteristické zvětšení ledvin a dilatace vývodného systému. Změny začínají již před 10. týdnem těhotenství. Každá ledvina se prodlužuje o 1–1,5 cm při současném zvýšení váhy. Pánvička je dilatována až do objemu 60 ml, když její objem u netěhotné ženy je okolo 10 ml. Uretery jsou dilatovány před vstupem do malé pánve, více vpravo než vlevo, jsou vinuté a prodloužené, ale jejich uskřinutí se vyskytuje velmi zřídka. Zvyšuje se stáza moče. Příčina hydronefrózy a hydroureterů není známá. V úvahu připadá několik faktorů: 1. zvýšená koncentrace progesteronu, která způsobuje snížení tonu hladkého svalstva ureterů (avšak hydroureter nevzniká při zvýšené tvorbě progesteronu u netěhotných), 2. rozšíření venózních ovariálních pletení v oblasti ligamentum suspensorium ovarii, 3. dextrotorze dělohy, která více komprimuje pravý ureter, 4. hyperplazie hladkého svalstva v distální části ureterů, která způsobuje zúžení lumina s následnou dilatací ureterů v kranilání části. Stáza moče je příčinou zvýšené pohotovosti k infekci vývodného systému močového (asymptomatická bakteriurie, pyelonefritida).
Ledvinové funkce
V těhotenství se ledvinové funkce mění zejména vlivem zvýšené produkce a sekrece některých mateřských a placentárních hormonů (ACTH, ADH, aldosteron, kortizol, hPL) a následkem zvětšeného objemu plazmy. Glomerulární filtrace (GF) se zvyšuje již od začátku těhotenství, od II. trimestru je to asi o 50 %, na konci těhotenství klesá a hodnot před těhotenstvím dosahuje za 20 týdnů po porodu. Průtok plazmy ledvinou se zvyšuje od začátku těhotenství, ve II. trimestru až o 25–50 %. V posledních týdnech před porodem se zvyšuje až o 75 % ve srovnání s hodnotami před těhotenstvím. Někteří autoři však prokázali, že průtok plazmy ledvinou se na konci těhotenství již nezvyšuje, ale zůstává stejný, nebo se dokonce o něco snižuje. Koncentrace Na+ je v tělesných tekutinách o něco snížena a následkem toho je snížena i osmolalita plazmy. Při zvýšené GF a zvýšených koncentracích progesteronu se zvyšuje pohotovost ledvin k vylučování Na+, tento stav je kompenzován zvýšenou reabsorpcí Na+ v tubulech, která je způsobena zvýšenými hladinami aldosteronu, estrogenů a desoxykortikosteronu. Přestože je GF v těhotenství výrazně zvýšená, množství moče se nezvyšuje. Vylučovací systém pracuje v těhotenství v tomto smyslu efektivněji než u netěhotných žen. Během těhotenství se zvyšuje clearance a snižují se plazmatické koncentrace močoviny, kreatininu, kyseliny močové, glukózy a aminokyselin. Koncentrace kreatininu klesá v I. trimestru ze 73 na 65 µmol/l, ve II. trimestru na 51 µmol/l a na konci těhotenství dosahuje hodnot okolo 47 µmol/l. V důsledku nižšího odbourávání proteinů a zvýšené clearence klesá plazmatická koncetrace močoviny. Respektování těchto fyziologických změn je důležité pro včasné odhalení renální nedostatečnosti v těhotenství. Jestliže je hladina kreatininu v pokročilém těhotenství nad 75 µmol/l a močoviny více než 5,4 µmol/l, jsou nezbytně nutná doplňující vyšetření renálních funkcí a vývodných močových cest.
Systém renin–angiotenzin–aldosteron
Renin je enzym, který se tvoří hlavně v juxtaglomerulárním aparátu v ledvinách a určité množství také v děloze. V těhotenství se jeho aktivita zvyšuje 5–10krát. Renin působí na substrát angiotenzinogen (produkovaný v játrech) a vzniká angiotenzin I a pak angiotenzin II, který má silné vazokonstrikční účinky. Hodnoty angiotenzinogenu i angiotenzinu I a II jsou v těhotenství pětkrát vyšší než u netěhotných, ale u žen s fyziologickým těhotenstvím vazokonstrikce nenastává. Tyto ženy jsou rezistentní na působení angiotenzinu v důsledku zvýšené aktivity leucin-aminopeptidázy, která štěpí angiotenzin II a tak zabraňuje jeho působení na cévní stěnu. Zvýšené hodnoty angiotenzinu II jsou příčinou zvýšeného krevního tlaku při preeklampsii, neboť tyto ženy na působení angiotenzinu II nejsou rezistentní. Angiotenzin II stimuluje také sekreci aldosteronu v kůře nadledvin. Vysoká koncentrace reninu byla zjištěna v plodové vodě. Význam není jasný.
Glykosurie
Glykosurie není v těhotenství neobvyklá a nemusí být známkou poruchy metabolismu cukru (diabetes mellitus). Glykosurii můžeme zjistit až u 50 % těhotných žen. Její příčinou je omezená kapacita resorpce proximálního tubulu pro glukózu při zvýšené GF v těhotenství. V těhotenství nemusí množství vylučované glukózy odpovídat hladině glukózy v krvi. Zvýšené množství glukózy v moči je jedním z faktorů, které zvyšují citlivost vylučovacího systému k infekci. Malé množství glukózy vylučují močí i zdravé netěhotné ženy, ale běžným vyšetřením se nezjistí (50–150 mg glukózy/24 h).
Proteinurie
Množství proteinů v moči se v těhotenství mění jen nepatrně. Zdravá netěhotná žena ztrácí 200–300 mg bílkovin za 24 h. Toto množství bílkovin nelze screeningovými metodami prokázat. Zvýší-li se ztráta na 500 mg/24 h a více, je již nutné pátrat po příčině, neboť proteinurie může být prvním příznakem patologického procesu. Zdravá těhotná žena může ve zvýšeném množství vylučovat i další látky, jako aminokyseliny, vitaminy rozpustné ve vodě (vitamin B12, acidum folicum) a cukry (laktózu, xylózu a fruktózu). Příčina není známá.
Močový měchýř
První známky anatomických změn nastávají okolo 4. měsíce těhotenství. Při zvětšování dělohy, hyperémii pánevních orgánů a hyperplazii svalů a pojivové tkáně močového měchýře se elevuje trigonum a zmenšuje se předozadní průměr. Intravezikální tlak se zvyšuje dvakrát a pro zachování kontinence se současně zvyšuje i maximální intrauretrální tlak. Snižuje se tonus hladkého svalstva měchýře, v důsledku toho se může zvýšit jeho kapacita až na 1500 ml. Při zvýšeném intravezikálním tlaku je močení častější.
5. Gastrointestinální systém
V těhotenství se zvyšují požadavky na výživu včetně minerálů a vitaminů, neboť část energie získané potravou předává matka vyvíjejícímu se plodu. Chuť k jídlu je v těhotenství obvykle větší, takže i příjem potravy je větší. Jedním z nejčasnějších příznaků těhotenství je nauzea a zvracení, event. ranní nevolnosti, které se objevují mezi 4. a 8. týdnem a ustávají asi v polovině II. trimestru. Etiologie není známá, je však dávána do souvislosti se zvýšenou hladinou progesteronu a hCG a se sníženým tonem hladkého svalstva žaludku. Těhotné s těmito obtížemi mají sníženou chuť k jídlu, snížený příjem potravy, někdy nastává i úbytek na váze a nutnost parenterální výživy.
Dutina ústní
V dutině ústní se zvyšuje tvorba slin, může se snížit pH a zvyšuje se kazivost zubů. Zvýšená kazivost zubů v těhotenství není způsobena snížením obsahu kalcia v zubech, neboť dentin není vaskularizován, a proto ani metabolizován (na rozdíl od kostí, kde je kalcium v těhotenství mobilizováno). Dásně jsou hyperemické, hypertrofické, často křehké a snadno po malých traumatech krvácejí. Může to být způsobeno zvýšenou hladinou estrogenů a nedostatkem vitaminu C. Někdy podobné příznaky pozorujeme i při dlouhodobém podávání orálních kontraceptiv. Úprava dásní do stavu před těhotenstvím nastává obvykle na začátku šestinedělí.
Gastrointestinální systém
Střevní motilita je v těhotenství snížena v důsledku zvýšené hladiny progesteronu, který způsobuje snížení tvorby motilinu. Motilin je hormon peptidové povahy stimulující tonus hladkého svalstva žaludku a střeva. Vyprazdňování žaludku je zpomaleno, zvyšuje se tvorba gastrinu (tvoří se také v placentě), následkem toho se zvyšuje objem žaludku a snižuje se jeho pH. Doba potřebná k průchodu potravy trávicí trubicí je v těhotenství prodloužena, důsledkem je zvýšené vstřebávání vody a častý výskyt zácpy.
Žlučník
Funkce žlučníku je těhotenstvím ovlivněna také. Snižuje se tonus hladkého svalstva stěny žlučníku, jeho vyprazdňování je zpomaleno, je neúplné, žluč je více vazká a zvyšuje se pohotovost k tvorbě žlučových kamenů.
Játra
V průběhu normálního těhotenství v játrech nenastávají morfologické změny, ale pouze změny funkční. Zvyšuje se aktivita alkalické fosfatázy (je pravděpodobně ovlivněna izoenzymy, které se tvoří v placentě), zvyšuje se tvorba cholesterolu, globulinů a fibrinogenu. Snižuje se produkce albuminu, a tak se snižuje i albumino/globulinový kvocient. Snižují se hodnoty nebílkovinného dusíku a kyseliny močové. Beze změn zůstává koncentrace 5-nukleotidázy, bilirubinu, transamináz a žlučových kyselin.
6. Reprodukční systém
Děloha
Hmotnost dělohy u netěhotné ženy je okolo 70 g a obsah dutiny děložní je menší než 10 ml. V době termínu porodu dosahuje hmotnost dělohy v průměru 1100 g a obsah dutiny děložní je 5–20 l, někdy i více. Rovněž se zvětšuje průsvit a počet krevních a lymfatických cév. U netěhotné ženy proudí dělohou méně než 2 % krve z minutového srdečního objemu, u těhotné v době termínu porodu asi 10 %, tj. 500–700 ml krve za minutu. Při růstu plodu se děloha zvětšuje, vystupuje z pánve a ukládá se spíše do pravé poloviny dutiny břišní (dextroverze) a rotuje doprava (levá hrana děložní leží blíže přední stěny břišní – dextrotorze). Příčinou této polohy dělohy je uložení rektosigmoidea v levé polovině pánve. Hrdlo děložní se za 4 týdny po koncepci stává měkčí a má lividní barvu. Tyto změny nastávají v důsledku zvýšené vaskularizace, edému spolu s hypertrofií a hyperplazií cervikálních žlázek. Mění se konzistence cervikálního hlenu; stává se vazkým a po natření na podložní sklíčko a zaschnutí má typickou krystalickou strukturu. Je to projev účinku progesteronu.
Ovarium
V těhotenství neprobíhá maturace folikulů a nenastává ovulace. Vzniká corpus luteum graviditatis, ve kterém se tvoří estrogeny, ale zejména progesteron. Progesteron produkovaný v corpus luteum je bezpodmínečně nutný k udržení těhotenství do jeho 8. týdne, potom je produkován v placentě. Tvorba progesteronu se po 8. týdnu v corpus luteum snižuje a v relativně malém a fyziologicky nevýznamném množství přetrvává až do konce těhotenství. Odstranění corpus luteum po 8. týdnu těhotenství nevede k abortu. Corpus luteum graviditatis a placenta produkují také relaxin. Lidský relaxin je peptid, který se skládá z řetězců alfa a beta, které mají téměř stejnou délku. Struktura relaxinu je podobná inzulinu a insulin-like growth factor I a II. Relaxin je detekovatelný dva týdny po koncepci a na rozdíl od progesteronu se jeho tvorba nesnižuje po 7. týdnu, ale trvá beze změn po dobu celého těhotenství. Relaxin není nutný k udržení těhotenství. Poslední studie prováděné na myších s delecí genu pro relaxin poukazují na jeho vliv na obsah tkáňové vody v symfýze (zvýšení), na obsah kolagenu v bradavkách, vagině, hrdle děložním a prsní žláze (snížení) a na proliferaci poševního a intracervikálního epitelu (stimulace). Relaxin má inhibiční účinek na kontrakci myometria a vazodilatační a angiogenní účinek na cévy. Těhotenský luteom je solidní ovariální pseudotumor složený z velkých luteinizovaných buněk. Není to nádor ve vlastním slova smyslu, neboť vzniká zvýšenou luteinizační reakcí ovaria a zaniká bezprostředně po porodu. Někdy se projevuje přechodnou virilizací matky (produkce androgenů). Plody ženského pohlaví jím však nejsou ovlivněny. Hyperreactio luteinalis je další pseudotumor ovaria, který vzniká v těhotenství. Vzniká ze stejných buněk jako luteom, ale je cystické konzistence. Po porodu spontánně zaniká.
Vagina a perineum
V těchto místech se zvyšuje prokrvení, prosáknutí a změkčení tkání. Sliznice pochvy je lividní – podobně jako u děložního hrdla, mukóza zesiluje a hypertrofují buňky hladkého svalstva. Zvyšuje se poševní sekrece, sekret je vazký, bílé barvy, pH je kyselé a kolísá v rozmezí 3,5–6. Je to způsobeno zvýšenou tvorbou kyseliny mléčné z glykogenu a účinkem Döderleinova laktobacilu.
7. Kožní systém
Kůže
Pavoučkové névy se objevují nejčastěji na hrudníku, obličeji a pažích. Kožní névy se v těhotenství zvětšují a tmavnou, po porodu se vracejí do původní podoby. U rychle rostoucích névů se doporučuje jejich okamžité odstranění. Asi u 50 % těhotných se objevuje palmární erytém, který ihned po porodu mizí. Příčinou je zvýšená tvorba estrogenů.
Striae gravidarum mají růžovou nebo purpurovou barvu, objevují se na stehnech, na prsou a v podbřišku. Jejich vznik není ovlivněn zvyšující se tělesnou hmotností, ale zvýšeným napětím kůže. Neznáme účinná preventivní opatření proti jejich vzniku a po skončení těhotenství nezanikají, jen jejich barva se mění na bílou.
Hyperpigmentace je zapříčiněna zvýšenou tvorbou estrogenů a melanocyty stimulujícího hormonu. Může se vyskytnout kdekoli na kůži, ale nejčastěji postihuje perineum a okolí pupku. Ve střední čáře v podbřišku tmavne linea alba a mění se na linea fusca. Kdekoli na kůži mohou vznikat tmavohnědé skvrny – chloasma. Po porodu nemusí všechny zcela zmizet.
Vlasy
U netěhotné ženy je asi 20 % vlasových folikulů v klidové fázi, u těhotných je to jen 10 %. Po porodu vstupuje více folikulů do klidové fáze, a to se projeví zvýšeným vypadáváním vlasů. Návrat do původního stavu nastává za 6–12 měsíců.
8. Prsy
V těhotenství se prsy zvětšují a připravují na laktaci. Zvyšuje se průtok krve prsy a některé ženy si stěžují na jejich zvýšené napětí a zvýšenou citlivost. Působením estrogenů se zvyšuje růst duktulů a progesteron podporuje hypertrofii alveolů. Zvětšuje se a tmavne areola mammae. Již od počátku těhotenství, ale zejména v jeho druhé polovině, může spontánně z prsů odtékat (nebo je možné vytlačit) vazkou žlutavou tekutina – kolostrum (mlezivo). Spontánní sekreci kolostra pozorujeme spíše u multipar. Vysoká hladina estrogenu v těhotenství brání prolaktinu ve vazbě na své receptory v prsní žláze – laktace je blokována. Hladina estrogenu po porodu prudce klesá, laktogenní účinek prolaktinu přestane být estrogenem inhibován a laktace obvykle začíná třetí poporodní den. Množství produkovaného mléka je závislé na krevním průtoku v prsní žláze. Pravá laktace se před porodem může vyskytnout u stavů spojených s poklesem hladin estrogenu (anencefalický plod, odúmrtí plodu aj.) nebo zvýšenou produkcí prolaktinu (nádor hypofýzy).
9. Zrak
Těhotné ženy si často stěžují na rozmazané vidění. Je to způsobeno edémem čočky a rohovky, který po porodu zaniká, a proto změny vizu není třeba korigovat. Během těhotenství je zvýšena drenáž komorové vody, což je spojeno s nižším nitroočním tlakem.
10. Endokrinní systém
Štítná žláza
Následkem zvýšené renální clearence jódu v těhotenství dochází ke snížení zásob jódu v organismu, a to i přes jeho dostatečný přísun potravou. Kompenzačně se zvětšuje štítná žláza a zvyšuje se vychytávání jódu. Tím je zajištěna dostatečná syntéza tyroidních hormonů, respektive eutyroidní stav organismu. Vysoká hladina estrogenu stimuluje tvorbu TBG (thyroid binding protein), proto interpretace klinických testů závislých na hladině TBG nebo na schopnosti štítné žlázy vychytávat jód musí být v těhotenství korigována.
Příštítná tělíska
V průběhu těhotenství je zapotřebí dodat plodu 25–30 g vápníku nezbytného k vývoji fetálních kostí, aniž by se narušila integrita kostních struktur matky. To je zajištěno souhrou aktivity parathormonu (PTH), kalcitoninu a vitaminu 1,25(OH)2D3. V těhotenství absorpci kalcia ve střevech podporuje zvýšená hladina vazebného proteinu pro vápník. Produkce PTH a hladina 1,25(OH)2D3 v plazmě je také zvýšena. Hladina ionizovaného vápníku v séru se nemění, ale klesá množství celkového vápníku následkem poklesu hladiny sérového albuminu.
Hypofýza
Přední lalok hypofýzy je v těhotenství 2–3krát zvětšený jako výsledek zmnožení prolaktin-secernujících buněk, stejně tak je zvýšená hladina prolaktinu. Dochází k poklesu hladiny gonadotropinů (FSH, LH) v důsledku vysoké hladiny estrogenu placentárního původu. Uvolňování růstového hormonu (GH) reagujícího na stimulaci argininem nebo hypoglykémií je utlumeno. Podle některých autorů také odpověď TSH na TRH může být pod vlivem estrogenu zesílena.
Nadledviny
Nadledviny se během těhotenství nezvětšují, i když stoupá produkce ACTH od I. do III. trimestru. Hladina kortizolu v plazmě stoupá v důsledku zvýšení hladiny vazebného globulinu pro kortikosteroidy, indukovaného vysokými hladinami estrogenu. Volný kortizol v plazmě má prodloužený poločas rozpadu.
11. Metabolismus
V důsledku rychlého růstu plodu a placenty a jejich zvyšujících se nutričních požadavků nastávají v těhotenství kvalitativní a kvantitativní změny metabolismu. Metabolické změny jsou ovlivňovány změnou produkce a sekrece některých hormonů u matky a tvorbou nových hormonů ve fetoplacentární jednotce a v neposlední řadě také transportem látek přes placentu. V těhotenství se zvyšuje spotřeba O2 a bazální metabolismus, ve III. trimestru až o 15–20 %.
Tělesná hmotnost
Přibývání tělesné hmotnosti v těhotenství je způsobeno růstem dělohy, placenty a plodu, zvětšením objemu prsů, krve a extravaskulární extracelulární tekutiny, v menší míře pak zvýšením objemu intracelulární vody, tuků a bílkovin. Průměrný přírůstek tělesné hmotnosti je na konci těhotenství 11–12 kg, v I. trimestru je to 1–2 kg, ve II. a III. trimestru vždy 5 kg (obr. 1). 1000 g z celkového přírůstku hmotnosti připadá na bílkovinu, z toho je 50 % transportováno do plodu a placenty.
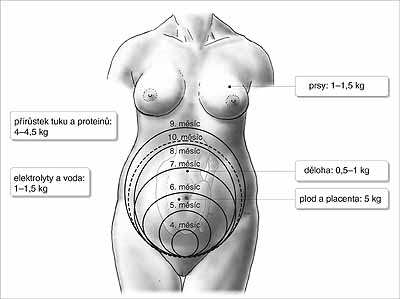
Obr. 1: Změny tělesné hmotnosti ženy během těhotenství a výška děložního fundu v jednotlivých měsících těhotenství
Metabolismus vody
V těhotenství se zvyšuje retence vody. Největší množství retinované vody je v období porodu (6,8 l). Jednou z příčin je změna osmotického prahu pro žízeň a zvýšení sekrece ADH, což vede ke snížení osmolality plazmy o 10 mOsm/kg. Další příčinou zvýšené retence vody je částečná okluze vena cava caudalis zvětšující se dělohou a edémy dolních končetin. K tvorbě edémů přispívá také snížený intersticiální koloidně osmotický tlak. Retinovaná voda může být využita při dehydrataci a k náhradě intravaskulární tekutiny při zvýšené ztrátě krve při porodu. Zdravá primipara, u které nebyly zjištěny edémy, snižuje svoji tělesnou hmotnost do 10 dnů po spontánním porodu v porovnání s dobou okamžitě po porodu v průměru o 2 kg. Příčinou úbytku hmotnosti nedělky je ztráta vody.
Metabolismus cukru
Zvýšená tvorba a sekrece některých hormonů (zejména placentárních) způsobuje, že těhotenství můžeme označit jako období, které je potenciálně diabetogenní. Těhotenství je charakterizováno hyperglykémií, hyperinzulinémií, hypertriglyceridémií a sníženou odpovědí na inzulin. Poločas inzulinu se v těhotenství nemění. Pro těhotenství je obvyklá snížená hladina glukózy nalačno a na druhé straně prodloužené období zvýšené hladiny glukózy po jídle. Jedním z důvodů snížené hladiny glukózy nalačno v těhotenství je její transport do fetoplacentární jednotky. Glukóza je primární zdroj energie pro plod a její hladina v plazmě plodu je závislá na hladině glukózy u matky. Plod není závislý na inzulinu matky, neboť jej začíná produkovat již v 9.–11. týdnu těhotenství a glykémie plodu je řízena inzulinem plodu. V těhotenství hypertrofují u matky b-buňky pankreatu a sekrece inzulinu se zvyšuje asi 2–3krát ve srovnání s netěhotnými. Placentární laktogen (hPL) způsobuje zvýšení rezistence periferních tkání a zejména jater na inzulin. Vzhledem k tomu, že se tvorba a sekrece hPL v průběhu těhotenství zvyšuje, zvyšuje se i rezistence na inzulin. Určitý význam pro metabolismus inzulinu a glukózy má inzulináza (štěpí inzulin), která je tvořena v placentě. Protiinzulinové, tedy diabetogenní účinky mají také volný kortizol a progesteron.
Metabolismus lipidů
Celková hladina tuků v plazmě se v těhotenství zvyšuje z 6 g/l na 10 g/l v závislosti na přírůstku tělesné hmotnosti. Ve 2. polovině těhotenství se zvyšuje koncentrace triglyceridů trojnásobně, fosfolipidů a cholesterolu o 50 %. Zvýšená hladina triglyceridů v plazmě vzniká na základě primárního zvýšení VLDL (very low density lipoprotein). Plazmatický low-density lipoprotein cholesterol (LDL-C) dosahuje nejvyšších hodnot v 36. týdnu, high density lipoprotein cholesterol (HDL-C) v 25. týdnu, pak jeho koncentrace v plazmě klesá a od 32. týdne se nemění až do konce těhotenství. Zvýšení LDL-C je způsobeno vlivem estrogenů a progesteronu na jaterní buňku. Pokles HDL-C po 25. týdnu je důsledek začátku rezistence na inzulin a jeho zvýšené koncentrace v plazmě v tomto období. V těhotenství se zvyšuje poměr LDL : HDL. Na začátku těhotenství je inhibována lipolýza, pravděpodobně v důsledku anabolického účinku inzulinu, v 2. polovině je však stimulována vlivem zvyšující se tvorby a sekrece hPL. Ve 2. polovině těhotenství, zejména ráno nalačno, se zvyšuje koncentrace volných mastných kyselin v plazmě (substrát pro energetický metabolismus matky), neboť glukóza a aminokyseliny jsou v této době ve zvýšeném množství transportovány k plodu, kde jsou utilizovány. Zvýšená hladina volných mastných kyselin v plazmě způsobuje zvýšenou tvorbu ketolátek (kyselina b-hydroxymáselná a acetoctová) a je příčinou zvýšeného rizika vzniku ketoacidózy, zvláště při delším hladovění. Po porodu nastává rychlý návrat k hodnotám před těhotenstvím.
Metabolismus proteinů
Pro těhotenství je charakteristická pozitivní dusíková bilance a hypoaminoacidémie. V posledních 6 měsících těhotenství se z potravy ukládá v průměru 5–6 g proteinů denně. Doporučuje se přijímat v tomto období okolo 60–75 g proteinů denně. Vedle příjmu proteinů je k uspokojení zvýšených energetických nároků v těhotenství nutné přijímat zvýšené množství energeticky bohatých potravin, tj. cukrů a tuků. V případě, že nejsou přijímány v dostatečném množství, zvyšuje se katabolismus bílkovin z mateřských zásob. Tyto proteiny jsou využívány pro krytí energetických nároků matky a plodu a nemohou být využity pro syntézu nových tkáňových proteinů. Aminokyseliny matky jsou snadno transportovány přes placentu k plodu a vzniká hypoaminoacidémie matky. Závažný je nedostatek alaninu, který je klíčovým prekurzorem pro glukoneogenezi v játrech matky. Koncentrace plazmatických proteinů se na konci těhotenství snižuje na 60–65 g/l, přičemž průměrná koncentrace proteinů u netěhotných žen je 70 g/l. Vzhledem ke zvýšenému objemu plazmy v těhotenství se celkové množství těchto látek v cirkulaci zvyšuje o 80 g. Koncentrace IgG, IgA a IgM v plazmě mírně klesá, naopak hladiny a1-antitrypsinu, a2-makroglobulinu, ceruloplazminu a transferinu jsou zvýšené. Koncentrace C3 komplementu a haptoglobinu se nemění. Změny plazmatických hodnot dalších proteinů jsou uvedeny v odst. 5 – Játra.
12. Vitaminy
Metabolismus kyseliny listové
Kyselina listová je esenciální pro syntézu purinů a pyrimidinů, a tím pro syntézu DNA. Dále hraje důležitou roli při množení a diferenciaci buněk. Denní potřeba kyseliny listové roste během těhotenství ze 400 µg/den na 800 µg/den. Dostatečný přívod bývá zajištěn přísunem 300–500 µg/den. Dosud chybí důkaz pro význam profylaktického podání kyseliny listové, s výjimkou oblastí s podvýživou – v těchto případech pak vede ke zvýšení porodní hmotnosti novorozence. V těhotenství hladina kyseliny listové v séru klesá, ale naopak stoupá v erytrocytech.
Metabolismus vitaminu B12
Koncentrace vitaminu B12 rychle klesá z 205–1025 ng/l před těhotenstvím na 20–510 ng/l na konci těhotenství. Pokles pravděpodobně souvisí s účinkem estrogenů. U kuřaček je pokles výraznější. Pro pokrytí denní potřeby vitaminu B12 je nutný průměrný denní přísun cca 3 mg. Obecně tuto potřebu plně kryje vyvážená strava. U vegetariánek může vzniknout deficit vitaminu B12, zde je pak nutná substituční terapie.
Další vitaminy
Sérová koncentrace retinolu, thiaminu a pyridoxal-5-fosfátu během těhotenství klesá. Sérová koncentrace riboflavinu a α-tokoferolu klesá nebo se nemění. Hladina vitaminu 1,25(OH)2D3 v plazmě je zvýšená.
13. Acidobazická rovnováha (ABR)
Acidobazický stav organismu je určen koncentrací vodíkových iontů [H+] v tělních tekutinách. Vzhledem k jejich nízkým hodnotám je vyjadřována jako pH (pH = –log [H+]). Normální pH arteriální krve je 7,40 ± 0,02 ([H+] = 38–42 nmol/l). Rozmezí pH arteriální krve, při kterém je možný život, je 6,8–7,8 ± 0,1 (10–160 nmol/l). V porovnání s arteriální krví je pH smíšené venózní krve nižší o 0,02–0,05, intersticiální tekutiny o 0,03–0,015. Intracelulární pH kolísá v rozmezí 6,0–7,3.
Produkce H+
Normální metabolické procesy produkují stále vodíkové ionty. Koncovým produktem karbohydrátů, tuků a aminokyselin je oxid uhličitý (CO2), který při reakci s vodou tvoří nestabilní kyselinu uhličitou (H2CO3). Ta dále disociuje na:
CO2 + H2O ↔ H2CO3 ↔ H+ + HCO3-
Kyselina uhličitá je ve formě CO2 vydýchána plícemi (viz níže). Do tělních tekutin je tímto způsobem denně produkováno přibližně 10 000 mmol H+.
Menší množství tzv. fixních kyselin vzniká při metabolismu bílkovin obsahujících síru (kyselina sírová) a při oxidaci bílkovin, tuků a nukleových kyselin obsahujících fosfor (kyselina fosforečná). Množství fixních kyselin tvořených za 24 h je závislé na druhu diety, v průměru je to 500–1000 mmol H+.
Při patologických stavech se v tělních tekutinách mohou hromadit organické kyseliny tvořené katabolismem tuků a cukrů, které se normálně rozkládají na CO2 a H2O. Např. při hypovolemickém či jiném cirkulačním šoku se může koncentrace kyseliny mléčné v tkáni výrazně zvýšit v důsledku nedostatečné tkáňové perfúze a aktivací anaerobní glykolýzy (laktátová acidóza).
Regulace pH
Udržování úzkého rozmezí pH je životně důležité. Organismus má velmi účinné regulační mechanismy, kterými se brání změnám pH. Stabilita pH vnitřního prostředí je zajišťována nárazníkovými systémy, respirační a renální regulací.
Extra- a intracelulární nárazníkové systémy umožňují rychlé chemické pufrování kyselin a bází. Rozlišujeme dva základní typy:
- bikarbonátový nárazníkový systém,
- nebikarbonátové nárazníkové systémy.
Bikarbonátový nárazníkový systém má největší význam, protože koncentrace jeho složek může být měněna podle potřeb organismu účinnými mechanismy respirace a vylučováním ledvinami. Systém je složen ze slabé kyseliny uhličité a konjugované báze, bikarbonátu . H2CO3 disociuje na H+ a HCO3- (rovnici viz výše). Jsou-li k roztoku H2CO3 přidány ionty H+, rovnováha se posunuje doleva a H+ ionty jsou z roztoku odnímány. Jsou-li přidány ionty OH-, vytvářejí spolu s H+ vodu a disociuje se další molekula H2CO3. H2CO3 je v dynamické rovnováze s CO2 rozpuštěným v krvi a v tělesných tekutinách. Rozpuštěný CO2 je pak v rovnováze s CO2 v alveolárním vzduchu, což činí z bikarbonátového nárazníkového systému otevřený systém.
Za fyziologického pH krve 7,4 je poměr koncentrací bikarbonátu sodného a kyseliny uhličité (+ rozpuštěného CO2) 20 : 1, protože:
Tzv. standardní bikarbonát = koncentrace bikarbonátů v plazmě nasycené kyslíkem, při teplotě 37 °C a při PCO2 40 torrů (5,32 kPa). Jde o koncentraci bikarbonátů při vyloučení respiračních vlivů vyjadřující míru alkalické rezervy krve. Normální hodnoty jsou 21–25 mmol/l. Tzv. aktuální bikarbonát představuje koncentraci bikarbonátů v 1 litru krve nasycené kyslíkem při aktuálně naměřeném PCO2.
Nebikarbonátové nárazníkové systémy:
- bílkoviny – mohou reverzibilně vázat H+ a OH- a fungují jako pufry, za normálního pH má bílkovina negativní náboj a působí jako báze;
- hemoglobin – za normálního pH působí jako kyselina, jeho nárazníková schopnost je dána přítomností imidazolové skupiny histidinu, která může vázat a uvolňovat H+;
- fosfáty – v plazmě se uplatňuje střední stupeň disociace kyseliny fosforečné; význam tohoto nárazníku je v plazmě malý, organické fosfáty jsou výrazným intracelulárním nárazníkem.
Celkové množství nárazníkových zásad, které mohou přijímat H+ v krvi, se nazývá sdružené nárazníkové báze (buffer base – BB). Normální hodnoty jsou 46–52 mmol/l krve nasycené kyslíkem. Tzv. přebytek zásad (base excess – BE) označuje množství zásad, které je třeba ubrat nebo přidat (u alkalózy nebo acidózy) k 1 litru krve nasycené kyslíkem při PCO2 40 torrů (5,32 kPa), aby se pH vrátilo k normě (tj. 7,4). Normální hodnoty jsou ± 2,3 mmol/l.
Respirační regulace
Periferní (glomus caroticum a oblouk aorty) a centrální (dechová centra) chemoreceptory reagují na změny PCO2, O2 a pH krve a míšního moku. Zvýšení PCO2, event. pokles pH zvyšují plicní ventilaci a naopak. Změny ventilace mohou měnit PCO2 v alveolech, který je v rovnováze s PCO2 v arteriální krvi. CO2 spolu s vodou tvoří kyselinu uhličitou, která částečně disociuje:
CO2 + H2O ↔ H2CO3 ↔ H+ + HCO3-
Změny alveolárního PCO2 mění proto rovnováhu rovnice: zvýšení alveolárního PCO2 (hypoventilace) posunuje reakci zleva doprava, takže dojde ke zvýšení H+ a opačně.
Renální regulace
Ledviny se podílejí na udržování acidobazické rovnováhy pomocí vylučování iontů H+ a pomocí vylučování a reabsorpce bikarbonátů. V těhotenství je snížen renální práh pro vylučování bikarbonátů.
ABR v těhotenství
Zdravá těhotná žena hyperventiluje ve srovnání s netěhotnou, a to způsobuje snížení PCO2 a respirační alkalózu. Respirační alkalóza je kompenzována metabolickou acidózou. Koncentrace plazmatického bikarbonátu se snižuje z 25–26 mmol/l na hodnoty okolo 22 mmol/l, snižuje se i koncentrace sdružených nárazníkových bází (buffer base). Výsledkem je minimální zvýšení pH. Zvýšení pH v krvi způsobuje posun disociační křivky hemoglobinu pro kyslík doleva a zvýšení afinity mateřského hemoglobinu pro kyslík (Bohrův efekt). Uvolňování kyslíku v mateřské krvi se snižuje. Hyperventilace způsobující snížení PCO2 u matky zvýhodňuje transport CO2 od plodu k matce, ale zdá se, že se zhoršuje uvolňování a transport kyslíku od matky k plodu. Mírné zvýšení pH mateřské krve v důsledku transportu CO2 od plodu k matce stimuluje produkci 2,3-difosfoglycerátu v erytrocytech matky, což má za následek zrušení Bohrova efektu a posun disociační křivky doprava, a tak je zvýhodněno uvolňování kyslíku z hemoglobinu matky a transport kyslíku od matky k plodu.
14. Centrální nervový systém
Emocionální, sociální a kulturní faktory přispívají k rozvoji psychologického stavu ženy během těhotenství a porodu. Těhotenství představuje stresující zkušenost a způsobuje rozsáhlé změny nálady během těhotenství, porodu a zejména v šestinedělí. Za hormonální základ pro emocionální labilitu bývá považován progesteron a endogenní opioidy. Naopak snížená enzymatická degradace opioidů v termínu porodu přispívá ke zvýšení prahu bolesti.
15. Muskuloskeletální systém
Relaxin produkovaný placentou a corpus luteum pravděpodobně stejně jako u zvířat může specificky ovlivnit vazivový aparát inhibicí syntézy kolagenu, což je potencováno zvýšenou aktivitou kolagenázy. Dochází hlavně k rozvolnění ligament pánevního pletence a páteře, což spolu s hmotností těhotné dělohy zvyšuje v těhotenství lumbální lordózu.
16. Fyziologické změny v průběhu porodu
Kardiovaskulární systém
Srdeční výdej v průběhu aktivního porodu stoupá přibližně dvojnásobně ve srovnání s hodnotami před porodem. Maximální vzestup je patrný v době bezprostředně po porodu. Příčiny vzestupu srdečního výdeje jsou multifaktoriální. Bolest a strach během porodu zvyšují mateřské cirkulující katecholaminy, s následnou tachykardií a zvýšením systolického objemu. Kontrakce dělohy způsobují cyklickou redistribuci krve do oběhu (autotransfúzi), což zvětšuje předpětí (preload) oběhu a zvýšení srdečního výdeje na základě Frank-Starlingova principu.
Respirační systém
Hyperventilace při porodu je fyziologická a představuje přirozenou odpověď na bolest. K hyperventilaci vedou kromě bolesti i špatné dechové techniky a strach. Hyperventilace způsobená průběhem děložní činnosti vede ke zvýšení dechového objemu na 750 ml a ke zvýšení dechové frekvence na více než 30 dechů/min. Minutová ventilace v průběhu děložních kontrakcí činí cca 26 l/min. Hodnoty maximálního proudění vdechovaného vzduchu jsou 20–34 l/min. Dechové parametry souvisejí s intenzitou porodních bolestí. Po podání porodnické analgezie jsou patrné významné změny. Po podání inhalační analgezie klesá ventilace na 18 l/min. Spotřeba O2 je v mezikontrakčním období cca 2,2 ± 0,3 ml/kg/min, zatímco během bolestivé kontrakce je 4,4 ± 0,6 ml/kg/min. Hyperventilace během porodu vede ke snížení mateřského PCO2 a může způsobit nebezpečnou respirační alkalózu s hypokapnií. Na hypokapnii reaguje arteriální systém dělohy vazokonstrikcí, takže hrozí placentární hypoperfúze. Následkem mateřské hyperventilace pak může vzniknout fetální hypoxémie.
Literatura
1. CIKOT, RJ., STEEGERS-THEUNISSEN, RP., THOMAS, CM., et al. Longitudinal vitamin and homocysteine levels in normal pregnancy. Br. J. Nutr., 85, 2001, p. 49–58.
2. CREASY, RK., RESNIK, R. Maternal-Fetal Medicine, Principles and Practice. Philadelphia : W. B. Saunders, 1984, p. 1–1147.
3. CUNNINGHAM, FG., MACDONALD, PC., GANT, MF. Williams Obsterics. Norwalk : Appleton and Lange, 1993, p. 1–162.
4. GUYTON, AC. Textbook of Medical Physiology. 8th ed. Philadelphia : W. B. Saunders, 1991, p. 1–1170.
5. HYTTEN, FE., LIND, T. Diagnostic Indices in Pregnancy. Basel : Ciba-Geigy, 1973, p. 1–122.
6. WHELAN, J. Relaxin: a potential new treatment for vasoconstrictive disorders. Drug Discovery Today, 2000, 5, p. 438–439.
7. LEE, JC., HAYASHI, RH., SHEPARD, MK. Fetal hemoglobin in women with normal and with hydatidiform molar pregnancy. Am. J. Hematol., 13, 1982, 2, p. 131–139.
8. MOORE, PJ. Maternal Physiology during Pregnancy. In DECHERNEY, AH., PERNOLL, M. Current-Obstetrics and Gynecology, Diagnosis and Treatment. USA : Lange Medical Book, 1994, p. 146–154.
9. STAMATOYANNOPOULOS, G., VEITH, R., et al. Induction of fetal hemoglobin by cell-cycle-specific drugs and recombinant erythropoietin. Am. J. Pediatr. Hematol. Oncol., 1990, 12, p. 21–26.
10. TRÁVNÍČEK, T., et al. Patologická fyziologie. Učebnice pro lékařské fakulty. Praha : Avicenum, 1987, s. 185–232.
11. UNEMORI, EN., ERIKSON, ME., ROCCO, SE., et al. Relaxin stimulates expression of vascular endothelial growth factor in normal human endometrial cells in vitro and is associated with menometorrhagia in women. Hum. Reprod., 1999, 14, p. 800–806.
12. WASSERSTRUM, N. Maternal Physiology. In HACKER, NF., MOORE, JG. Esentials of Obstetrics and Gynecology. Philadelphia : W. B. Saunders, 1992, p. 61–73.
13. WEINREB, RN., LU, A., BEESON, C. Maternal corneal thickness during pregnancy. Am. J. Ophthalmol., 105, 1988, 15, p. 258–260.
14. WEST, JB., et al. Physiological basis of medical practice. 12th ed. USA : Williams & Wilkins, 1990, p. 1–1170.
15. ZHAO, L., SAMUEL, CS., TREGEAR, GW. Collagen studies in late pregnant relaxin null mice. Biol. Reprod., 63, 2000, p. 697–703.
16. ZIAI, N., ORY, SJ., et al. Beta-human chorionic gonadotropin, progesterone, and aqueous dynamics during pregnancy. Arch. Ophthalmol., 112,1994, p. 801–806.
17. ŽIVNÝ, J. Doktorská disertační práce. II. díl, Praha, 1987, s. 141–284.
